Fabrication de chaufferettes chimiques
Sommaire
- 1 La théorie généraliste
- 1.1 Les acides et bases
- 1.2 L'endothermicité et l'exothermicité
- 1.3 La sursaturation
- 2 La théorie de la réaction
- 2.1 Mieux comprendre la réaction
- 2.2 Le rendement
- 2.2 Bilan des quantités de matière
- 2.2.1 L'acide acétique
- 2.2.2 Bicarbonate de soude
- 2.2.3 Acétate de sodium
- 3 La pratique
- 3.1 Matériel nécessaire
- 3.2 Protocole
Nous publions aujourd'hui avec grand plaisir l'article d'un lecteur de fire-DIY : Alchimiste. C'est son premier article sur le site sur un thème que nous n'avons encore jamais abordé, la chimie. Merci à lui.
Avec l'hiver à nos portes, quoi de mieux que de se réchauffer à l'aide de petites chaufferettes faites maison ? Pour cela rien de plus simple, et quelle excellente façon de s'initier à la chimie !
Je vais donc vous faire découvrir à travers ce tutoriel des simples notions de chimie inorganique et de thermochimie, et surtout vous donner un petit protocole facile de réalisation pour créer vos propres chaufferettes.
En premier lieux nous parlerons de la théorie générale (c'est à dire des notions de base, afin de mieux découvrir la chimie), puis de la théorie de la réaction (nous aborderons ici les caractéristiques des réactions se déroulant durant le protocole) et enfin de la pratique (on est là pour ça, quand même!), donc rien ne vous interdit de passer directement à la partie pratique !
Je n'ai pas inventé ce protocole, mais le sujet m'a semblé sympas pour un premier tuto, enjoy !
1 La théorie généraliste
C'est bien beau de réaliser un protocole, mais quitte à s'y mettre, autant le comprendre ! Aussi je vais tenter de vulgariser dans cette première partie quelques notions de chimie.
1.1 Les acides et bases
Qu'est ce qu'un acide, qu'est ce qu'une base ? Comme vous le savez déjà sûrement, la matière est constituée de molécules, elles mêmes constituées d'atomes liés entre eux par (entre autres) des liaisons covalentes caractérisées par un partage équitable d'électrons.
Par exemple, la molécule d'eau ($H_2O$) est constituée de deux atomes d'hydrogènes (pouvant partager un électron) liés à l'oxygène (pouvant partager deux électrons) étant l'atome central. La géométrie de la molécule ressemble donc à l'image ci dessous :
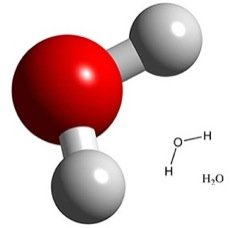
Mais pourquoi tu nous parles de la molécule d'eau pour nous parler d'acide ?
D'après la définition du chimiste Danois Joannes Bronsted (1879-1945), un acide est une espèce chimique capable de céder un proton (c'est à dire de libérer un atome d'hydrogène , noté $H^{+}$, en brisant la liaison covalente), une base quand à elle, est une espèce capable de capter un proton.
A la lumière de ces définitions, il est donc possible de définir l'eau comme :
- Un acide : la molécule d'eau $H_2O$ peut céder le proton $H^{+}$ à l'espèce $HO^{−}$. En effet : $$(HO^{−}) + (H^{+})=(H_2O)$$
- Une base : la molécule $H_2O$ peut également capter le proton $H^{+}$ à l'espèce $H_3O^{+}$. En effet : $$(H_2O) + (H^{+}) = (H_3O^{+})$$
Mais si l'eau est un acide, pourquoi ne meurt-on pas à la moindre gorgée ?
Voilà ce à quoi je voulais en venir : les différents types de bases et d'acides, c'est à dire les forts, les faibles ou les indifférents.
Un acide est caractérisé par sa réaction avec l'eau :
- Un acide (ou une base) forte est un composé suffisamment instable pour réagir totalement avec l'eau, c'est à dire que cette réaction admet un équilibre tel qu'il ne reste plus d'acide (ou de base) dans le milieu réactionnel
- Un acide (ou une base) faible réagit de telle manière qu'il reste une grande quantité de matière dans le milieu réactionnel, elle ne réagit donc pas totalement avec l'eau
- Un acide (ou une base) indifférente ne réagit pas avec l'eau (c'est donc évidemment le cas du $H_2O$, il n'y a pas de réaction entre l'eau et l'eau !)
Voilà, vous savez tout sur les composés acido-basiques ! Je voulais expliciter cette partie puisque ces termes reviendrons plusieurs fois dans mes futurs tutos !
1.2 L'endothermicité et l'exothermicité
Voilà une autre notion qui va nous être utile pour mieux comprendre comment marche la chaufferette.
Certaines réactions sont caractérisées comme exothermiques ou endothermiques :
- Une réaction chimique est exothermique (comme les réactions acido-basiques) si elle engendre la création de chaleur, en d'autres termes, si elle "chauffe". Cet échauffement est dû au fait qu'il sera, dans ce type de réaction, plus coûteux en énergie de détruire les liaisons des réactifs que de former celles des réactifs, la différence d'énergie sera donc transformée en chaleur.
- Une réaction endothermique est l'opposée d'une réaction exothermique, c'est à dire qu'elle absorbe de la chaleur, en d'autres termes une fois encore, elle "refroidit". Un bon exemple est la détente d'un gaz : gonflez un ballon de baudruche, ouvrez le ensuite pour laisser s'échapper l'air et touchez le ballon dégonflé : ce dernier aura refroidit.
Voilà de nouvelles définitions qui reviendrons dans les tutos, et étant la base de celui ci.
1.3 La sursaturation
Imaginons : Lorsque l'on dissout du sel dans de l'eau, nous pouvons remarquer que le sel se dissout jusqu'à une certaine limite, à partir de laquelle le sel ne se dissout plus dans l'eau et forme un dépôt au fond du verre : on introduit alors le concept de solubilité.
Ainsi, la solubilité d'un soluté dans un solvant correspond à la concentration maximale de soluté pouvant se dissoudre dans le solvant avant saturation du mélange.
Une des particularité de la solubilité, c'est qu'elle augmente avec la température. En effet, pour reprendre notre exemple précédent, la masse de sel pouvant se dissoudre dans le même volume d'eau va augmenter lorsque la température augmentera, le dépôt disparaîtra donc.
Maintenant imaginons un autre cas : Nous possédons de l'eau à 100°C, la masse maximale de sel pouvant se dissoudre est de 391g, mais si on laisse se mélange au repos, lorsque la température va baisser jusqu'à 25°C, la masse maximale ne sera plus que de 357g, soit 34g de différence; l'eau ainsi refroidie sera dans un état instable dit de sursaturation : la moindre perturbation va entraîner une cristallisation des cristaux présents dans solution. La sursaturation correspond donc à une concentration d'un soluté dans un solvant supérieure à celle maximale à une température donnée.
Voilà pour la théorie globale, utile uniquement si vous vous intéressez à la pure théorie de ce tuto, abordons à présent la théorie de la réaction, histoire de savoir pourquoi vous avez ingurgité toutes ces informations.
2 La théorie de la réaction
2.1 Mieux comprendre la réaction
Entre l'acide faible qu'est l'acide acétique (présent dans le vinaigre) de formule $CH_3COOH$ avec la base qu'est l'hydrogénocarbonate de sodium (plus connu sous le nom de bicarbonate de soude) de formule $NaHCO_3$ se produit une réaction acido-basique entraînant la formation d'acétate de sodium de formule $C_2H_3NaO_2$ selon l'équation bilan :
$$(CH_3COOH)_L + (NaHCO_3)_L = (C_2H_3NaO_2)_S + (H_2O)_L + (CO2)_G$$ L'indice L signifie "phase Liquide", l'indice S "phase Solide" et l'indice G "phase Gazeuse".
La cristallisation de l'acétate de sodium a la particularité d'être exothermique, pouvant ainsi engendrer des températures de l'ordre de 45°C durant une période pouvant aller jusqu'à 1h. Nous allons donc utiliser cette caractéristique de l'acétate de sodium pour créer nos petites chaufferettes, en utilisant le phénomène de sursaturation.
2.2 Le rendement
Cherchons ici à déterminer la masse d'acétate de sodium formée à l'issue de notre réaction. Mais avant tout, remettons dans nos têtes quelques points :
Proportions stœchiométriques : Les réactifs sont en proportions stœchiométriques si ils sont entièrement consommés en fin de réaction.
Réactif limitant : Lors d'une réaction (n'ayant pas des réactifs en proportions stœchiométriques), si l'un des réactif est entièrement consommé au point de stopper la réaction, alors il est caractérisé de réactif limitant.
Réaction totale : Notre réaction est totale, c'est à dire qu'à l'état d'équilibre (donc à la fin de la réaction), tous les réactifs (qu'ils soient en proportions stœchiométriques ou non) sont consommés (du moins il est possible de le considérer comme tel), j'expliquerais plus précisément dans un autre tuto comment savoir si une réaction est totale ou non.
Moles : La mole est une unité internationale et correspond à une quantité de matière : Une mole contient environs 6.02 mille milliard de milliard d'atomes (bon, ceci est a titre indicatif, pour la culture générale on va dire). L'unité est notée mol
Masse molaire : La masse molaire, exprimée en g/mol correspond à la masse d'une mole d'un composé.
Concentration molaire : Exprimée en mol/L, elle correspond a la concentration de moles dans un solvant donné
Avancement : L'avancement permet de caractériser, à un instant donné, le nombre de moles d'un constituant ayant été consommées (ou formées) entre l’état initial et l'état final.
Tableau d'avancement : Il consiste à "lister" les quantités de matière de chaque constituants entre l'instant initial et l'état final, afin d'avoir un meilleur point de vue sur la situation !
2.2 Bilan des quantités de matière
2.2.1 L'acide acétique
Nous partons donc avec 500mL de vinaigre. Or, pour un volume de vinaigre, seulement 6% correspond à de l'acide acétique, nous avons donc un volume de $500 \times 0.06 = 30mL.$
Sa masse volumique étant de 1.05g/mL, on a donc une masse de $1.05 \times 30 = 31.5g$
La masse molaire de l'acide acétique étant de 60g/mol, on a donc une quantité de matière de $\dfrac{31.5}{60} = \fbox{0.52mol}$
2.2.2 Bicarbonate de soude
La réaction se fait avec 35g de bicarbonate de soude, ayant une masse molaire de 84g/mol, on commence donc avec une quantité de matière initiale de $\dfrac{35}{84} = \fbox{0.41mol}$
2.2.3 Acétate de sodium
Pour calculer la quantité de matière d'acétate de sodium, nous allons tracer la tableau d'avancement de la réaction; on notera x l'avancement :
| Etat | $(CH_3COOH)_{L} + (NaHCO_3)_{L} \longrightarrow (C_2H_3NaO_2)_{S} + (H_2O)_{L} + (CO_2)_{G}$ | ||||
|---|---|---|---|---|---|
| Etat initial | 0.52 mol | 0.41 mol | 0 mol | 0 mol | 0 mol |
| Etat final | 0.52-x mol | 0.41-x mol | x mol | x mol | x mol |
On a donc créé x moles d'acétate de sodium, comme noté sur le tableau d'avancement. Or le bicarbonate de soude va ici être limitant : sa quantité de matière est inférieure à celle de l'acide acétique. La réaction étant totale, on en déduit que 0.41-x=0 donc que x=0.41mol. On obtient donc 0.41 moles d'eau, de dioxyde de carbone et d'acétate de sodium. Or la masse molaire de l'acétate de sodium étant de 82 g/mol, on forme donc théoriquement une masse de $82 \times 0.41 = 33.62g$ d'acétate de sodium.
3 La pratique
3.1 Matériel nécessaire
- 500mL de vinaigre blanc (0.5 Litres)
- 35g de bicarbonate de soude
- 500mL d'eau bouillante
- Un filtre à café
- Une cuillère
- Une casserole
- Un petit sachet devant être résistant et étanche
Voici un calculateur afin de vous simplifier les calculs des quantités de matière :
3.2 Protocole
Il est temps de passer à la pratique !
a) Mettre 500mL de vinaigre dans un récipient et ajouter doucement le bicarbonate de soude (Vous pourrez observer un dégagement gazeux par formation de mousse, c'est du dioxyde de carbone)

b) Verser cette solution dans les 500mL d'eau bouillante dans la casserole et laisser évaporer la solution (environ 90%): on remarque alors la formation de cristaux au fond de la casserole.

c) Enlever un léger surplus d'eau en filtrant la solution dans la casserole afin de garder un mélange de cristaux avec un peu d'eau.

d) Faire fondre le mélange à basse température dans la casserole

e) Verser la solution dans le sachet prévu à cet effet.

f) Laisser le sachet reposer à l'air libre en évitant tout choc.

g) Malaxer par la suite le sachet, pour entraîner la cristallisation d'acétate de sodium qui, étant exothermique, va nous fournir de la chaleur !

J'espère que ce tutoriel vous aura plus et qu'il aura permis à certains néophytes de s'initier à la chimie !
Vos réactions (0) :
- Sois le/la premier(e) à commenter cet article !

